齊魯制藥領跑一致性評價,復星醫藥幾乎全為289品種
據藥智藥品注冊與受理數據庫統計,截止12月6日,CDE共受理一致性評價受理號580個,涉及221家企業的210個品種。其中引人注目的是,在所有申報一致性評價的企業當中齊魯制藥無論是從受理號還是從品種數來看,都是申報最多的企業,申報受理號達44個,品種數有25個,高居申報一致性評價申報企業榜首;其次為復星醫藥24個受理號14品種,值得提及的是復星醫藥申報的14個品種有13個為289目錄藥品;中國生物制藥也以23受理號18品種緊隨其后,其中正大天晴占19個受理號15個品種(包括南京正大天晴)。以下是申報一致性評價審報企業TOP10詳情:
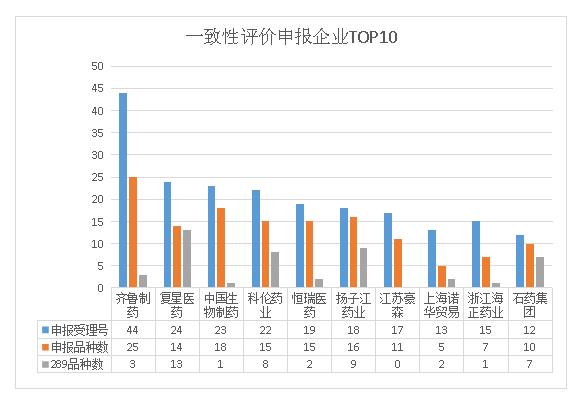
華海藥業一致性評價大贏家,石藥、揚子江、復星醫藥289過評最多
截止12月6日,共有126個受理號64個品種通過一致性評價(含視同通過),其中289目錄藥品有42個受理號21個品種過評,完成率僅7.27%。年關將至,各企業一致性評價工作通過情況如何?下面一起看看一致性評價通過較多的前5個企業詳情。
通過一致性評價企業TOP5
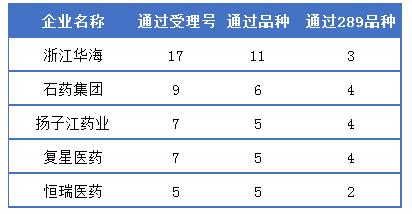
華海藥業通過一致性評價詳情
浙江華海藥業無疑是一致性評價的最大贏家,17受理號11品種過評。另據藥智藥品注冊與受理數據庫顯示,其中通過補充申請一致性評價受理號有10個,涉及8個品種,且為華海藥業申報的一致性評價所有藥品,目前全部過評,可謂百發百中;此外,還有7個受理號3品種,通過進入中國上市藥品目錄集,視同通過一致性評價;且在已過評的11品種中需要在今年年底完成的289目錄品種有3個,為鹽酸帕羅西汀片、利培酮片和奈韋拉平片,具體詳情可見下表:
華海藥業一致性評價獲批詳情表
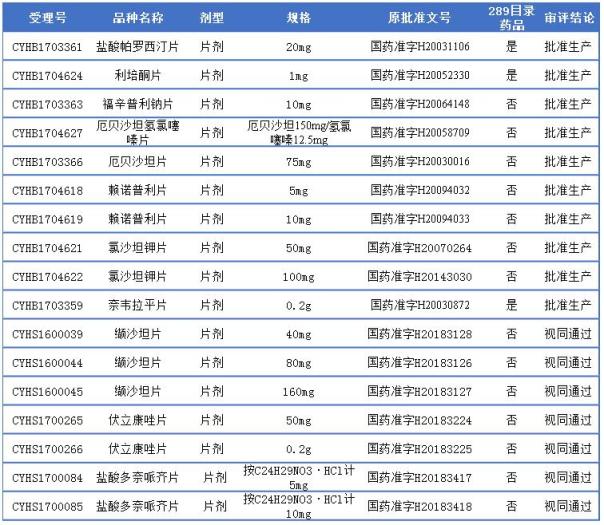
除了華海藥業,石藥集團、揚子江藥業、復星醫藥、恒瑞醫藥一致性評價也不甘落后,且值得提及的是石藥集團、揚子江藥業和復星醫藥盡管通過的品種數遠遠少于浙江華海藥業,然而他們的289目錄藥品卻是所有企業通過最多的,均有4個品種過評,占據各自企業通過品種數量的大半。
石藥集團過評一致性評價詳情
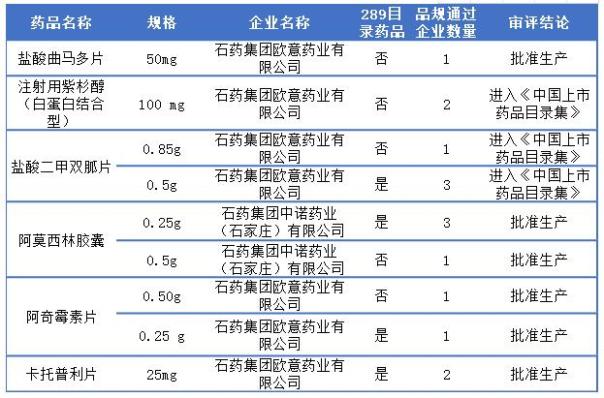
石藥集團的一致性評價藥品主要來源于石藥歐意和石藥中諾,其中石藥歐意占5個,289目錄藥品有3個,為鹽酸二甲雙胍片、阿奇霉素片和卡托普利片;石藥中諾有1個,為289目錄藥品阿莫西林膠囊;詳情如下表:
石藥集團通過一致性評價詳情表
揚子江藥業過評一致性評價詳情
揚子江藥業5個過評品種當中有4個藥品為289目錄藥品,為揚子江上海海尼藥業苯磺酸氨氯地平片、揚子江廣州海瑞藥業格列美脲片以及揚子江集團蒙脫石散和揚子江江蘇制藥馬來酸依那普利片,且其中馬來酸依那普利片和格列美脲片為首家過評品種,更多詳情可見下表:
揚子江一致性評價過評詳情表
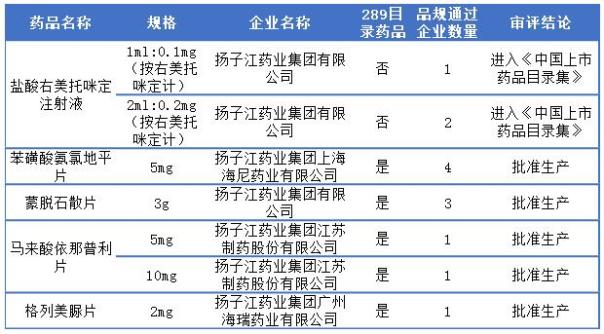
復星醫藥過評一致性評價詳情
復星醫藥一致性評價同石藥集團一樣,一致性評價藥品主要來源于旗下的子公司,且5個品種有4個為289目錄藥品,江蘇黃河的苯磺酸氨氯地平片、重慶藥友的阿法骨化醇片和鹽酸克林霉素膠囊以及蘇州二葉的阿奇霉素膠囊,且阿法骨化醇片和阿奇霉素膠囊目前為止僅有1家過評。更多詳情可見下表:
復星醫藥通過一致性評價詳情表
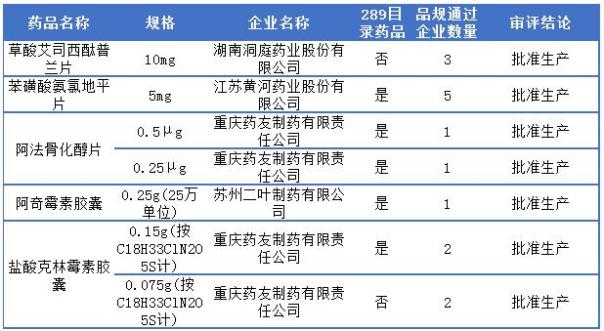
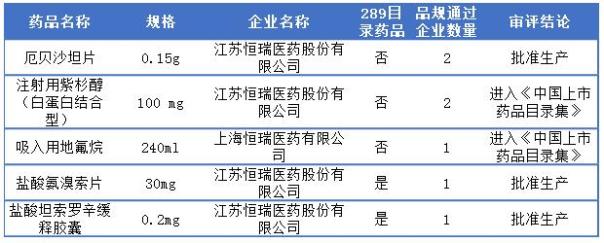
恒瑞醫藥一致性評價通過詳情
恒瑞醫藥截止目前一致性評價一共有5品種過評,其中江蘇恒瑞醫藥占4個,上海恒瑞醫藥僅1個,2個289目錄藥品為江蘇恒瑞的鹽酸氨溴索片和鹽酸坦索羅辛緩釋膠囊,更多詳情可見下表:
恒瑞醫藥通過一致性評價詳情表
2015年6月,醫生告訴69歲的帥水清(音),她患上了胃癌,需要做手術。她來到位于成都的華西醫院。這家醫院是在中國最好的醫院之一。她在那里為了排一位外科醫生的手術等了6周。到接受手術時,她已經陷入休克。外科大夫發現,癌細胞已經擴散到其他器官。她在一年后去世。
文章稱,很難說,早點做手術是否會拯救帥水清的性命。但她的例子揭示了中國一個越來越嚴重的問題,即病人對醫療的需求遠遠超過中國提供醫療的能力。病人往往要冒著風險等待很長時間才能接受手術。這不是因為中國缺乏外科大夫,而是因為實際上能做手術的外科大夫人數不足。世界銀行的數據顯示,中國人均擁有的外科醫生數量同其他中高收入國家相同,但總體來說,中國外科醫生進行的手術比其他國家外科醫生少40%。
手術產出為什么這么低?一個原因是親身實踐的培訓太少,當中國的外科醫生完成手術培訓,很多人很少有機會做手術。培訓后,他們可能會花很多年協助資深的外科大夫或從事一些簡單治療。2016年,中山大學的一些中國公共衛生專家在英國《柳葉刀》周刊上撰文說,在中國,不足5%的手術是由43歲以下的醫生完成的。他們寫道:“今天中國各個層次的外科受訓人員面臨的最大挑戰是親身學習的機會太少。”
文章稱,作為一名研究中國外科教育的美國醫學生,馬貢曾經在中國的時候已經了解了上述數據。美國體系有著“看一個、做一個、教一個”的風氣,在美國,醫學教育工作對醫生來說是最受尊敬的就業形式。所以,當馬貢來到中國,看到中國學術性醫學中心里實踐性教學之少依然讓他吃驚。馬貢發現,年輕外科醫生通常要花數十年才能等到機會停止旁觀、開始做手術。在美國,在一定安全和實踐約束之下,外科醫生會給予受訓者最大的自主權。
在中國,有關的學習被推遲了。舉北京一家一流醫院的一名眼科醫師的情況為例。獲得碩士和博士學位后,她完成了一個醫生實習項目。現在是一個著名眼科醫院的眼科主治醫生。除了她繁忙的培訓計劃,她還設法發表了數十篇同行評議的研究論文。我問她做過多少臺白內障手術。她說:“一臺也沒有。我看了很多臺手術,但從來沒有操作過。”她這個職業階段的美國眼科醫生就算沒有做過數百臺這類手術,也做過幾十臺了。
由于很多外科醫生只能在職業中期之后從事手術,這個體系制造的瓶頸會影響對病人的護理。例如,在中國,一半的失明病例源于沒有接受白內障手術,但卻只有36%的中國眼科醫生可以做手術。結果,中國人均白內障手術率比資源較貧乏的越南和印度還低很多,比起美國就更低得多。在美國,不足15%的失明病例源于白內障。
文章稱,高水平的外科醫生常常集中在大型醫學中心,這導致小醫院缺乏有經驗的醫生,而大醫院擠滿了尋求專業醫療的病人。北京協和醫學院的婦產科醫師龔曉明(音)說,這種情況導致一些鄉村病人冬天在寒冷的北京排隊等待幾天,只為做一個簡單的檢查。
]]>
吉林大學教授、同寫意新藥英才俱樂部理事長朱迅圖片來源:每日經濟新聞
今日(12月3日)下午,由每日經濟新聞主辦的“2018中國醫藥資本論壇”在廣州舉行,吉林大學教授、同寫意新藥英才俱樂部理事長朱迅出席論壇并發表了“醫藥崛起,來自每一次改革——新藥研發的中國機會”主旨演講。
朱迅提到,我國醫藥行業正在經歷的監管政策調整,不是一次局部的或者階段性的調整,而是一場全方位的變革,變革目的是重構。眼下,我國的監管政策正在向國際通用規則靠近,這將徹底改變我國制藥行業的商業模式。商業模式的變化之一就是制藥公司及藥品品種的格局將發生重塑,從銷售主導走向產品主導,“產品為王”的時代正在到來。
朱迅表示,我國醫藥行業藥品低門檻的時代即將結束,“今天我國大量的制藥公司,在十年后可能將不復存在。強者恒強、弱者離場的局面即將到來。”
]]>
人工心臟需求量大
心血管疾病已經成為國民第一位死亡原因,全國心血管疾病患者高達2.9億。每年大約有370萬人死于心血管疾病。目前心血管疾病的治療方式主要有藥物治療,外科手術治療和介入治療。心力衰竭患者以往只能等待心臟移植,而器官移植等待期往往較長,人工心臟的出現猶如“及時雨”,能幫助患者延長壽命。
中國醫學科學院阜外醫院再生醫學重點實驗室副主任周建業教授介紹,人工心臟分為輔助人工心臟和全人工心臟,我國所說的人工心臟是輔助人工心臟。其應用主要有三類,包括給等待心臟移植供體的患者提供過渡的時間和支持;或用于逆轉心臟重構、恢復患者心臟功能;或為患者提供終生的心臟輔助。從2006年6月至2018年7月,已經有近2.5萬人使用了輔助人工心臟,尤其是2013年以來,每年都會在2500人以上,需求很大。但是,人工心臟動輒上百萬元的費用也讓不少人為之咋舌。
對此,胡盛壽強調,只有發展國產人工心臟,才能降低治療費用。這也使得人工心臟研發成為心血管研發中非常重要的領域。而且人工心臟研發是所有心血管醫療器械研發中含金量最高、研發周期較長、需要多個學科共同參與的領域。
我國七個單位在研發人工心臟當前醫療器械是我國大健康領域創新最活躍、發展最強勁、動力最充足的產業之一。在國家各個方面的支持下,我國醫療器械創新能力有了顯著提升,新技術新產品也層出不窮,這其中就包括了人工心臟的研發。
周建業介紹,我國有七個單位在研發人工心臟,包括一代、二代和三代。新京報記者查詢資料發現,重慶永仁心醫療器械有限公司的離心泵型人工心臟技術由日本研發,是首個在中國獲批臨床試驗的人工心臟,已經完成11例注冊臨床試驗。由天津市蘭德投資有限公司和山西省長治市久安人工心臟科技開發有限公司共同研制的軸流泵型人工心臟也已經完成了5例臨床試驗,同樣是我國自主研發的人工心臟。而即將開始臨床試驗的是第三代全磁懸浮離心泵人工心臟,由江蘇同心醫療器械有限責任公司研發。
新京報記者從到會的江蘇同心工作人員處得到確認,目前人工心臟臨床試驗審批正在進行倫理審查,預計下周拿到臨床試驗批件,下月可以進入臨床試驗。胡盛壽介紹,該款人工心臟所有技術參數均達到了全球最先進的磁懸浮人工心臟技術指標,甚至有些方面更為優秀,比如體積更小、重量更輕。
除此之外,還有航天18所與天津泰達醫院、深圳核心醫療科技有限公司也在分別研發第三代人工心臟。前者仍在注冊檢驗階段,后者則處在樣機研發階段。
]]>

“有條件的地方可以探索區域共享網絡支付平臺建設。通過提供更加便捷的支付結算服務,優化就診流程,提高工作效率,提升服務質量。”近日,國家衛生健康委辦公廳印發《關于印發公立醫院開展網絡支付業務指導意見的通知》,以指導公立醫院開展網絡支付業務,進一步改善患者就醫體驗。
《通知》提出,要構建科學規范的網絡支付管理運行機制。首先要嚴格賬戶和資金管理。醫院財務部門統一負責網絡支付結算銀行賬戶使用和管理,切實履行資金存放管理責任,加強賬戶資金管理,保障資金安全。用于網絡支付業務結算的銀行賬戶,應當是以單位名義開設的銀行賬戶,賬戶的開立和使用符合財政部門、中國人民銀行和國家衛生健康委賬戶管理有關規定。
第二是要規范對賬和結算管理制度。醫院應當每日對網絡支付業務的賬務進行核對。如有差異,要及時查明原因,及時處理,確保醫院信息系統、銀行結算賬戶賬款保持一致。對于發生單邊賬項的情況,醫院應當明確處理流程,核實交易的真實性,確認交易最終完成后,再進行相應業務操作和賬務處理。
此外還在強化退費管理制度、建立檔案管理制度、完善信息系統管理制度、健全內部控制制度等方面提出了相應的建議和要求。
《通知》尤其指出要周密做好網絡支付業務開展前的評估論證。首先要對運用網絡支付業務的可行性進行充分論證。醫院在全面開展網絡支付業務前,應當結合自身實際情況,組織相關專家及技術人員論證選用商業銀行或非銀行支付機構(以下簡稱支付機構)的信息平臺是否能與現行的醫院信息系統相融合,評估醫院信息系統運行維護、安全技術防護等級是否達標等,充分考慮自身風險承受能力。
其次,要對合作機構資質嚴格審核。醫院應當嚴格審核合作商業銀行或支付機構資質,依據相關法律法規選定合作機構。在與支付機構合作時,應當對其《支付業務許可證》的許可范圍和有效期限進行查驗,并且優先選擇資質高、實力強、信譽好的機構。
此外,還要明確相關責任。醫院應當重視網絡支付業務的合同管理,組織法律、信息技術、財會、醫務等人員參與網絡支付服務的談判及合同訂立,應當就收單銀行結算賬戶的設置和變更、資金結算周期、結算手續費標準、差錯和爭議處理等事項,與支付機構、商業銀行明確權利、義務和違約責任。對于開通支付平臺公眾服務窗的情況,由于其中預約掛號、報告查詢、線上繳費等功能涉及患者信息和醫院業務數據等,應當要求服務商禁止以任何形式對外提供患者的身份及診療信息。
《通知》還強調要在加強對公立醫院開展網絡支付業務的指導、研究推行電子醫療收費票據的措施、協調推進網絡支付與醫保結算的對接等方面提出要求,以加強網絡支付業務開展后的業務指導和監督管理工作。
]]>6月8日,齊齊哈爾市相關部門在聯合檢查中發現訥河市某藥店出售假藥“舒筋健腰丸”,接著又陸續在依安縣、甘南縣、克山縣等地多處藥店、診所查獲大量假藥。
此案件引起了公安部及最高檢的高度重視。由此,一場打擊假藥的行動由此展開。此次案件中,公安部迅速成立“6·8”專案組督辦此案,而最高檢也將其列為掛牌督辦的案件。在河南、黑龍江兩省公安機關的配合下,李某和另外4個制假團伙被抓獲歸案,13個銷售假藥犯罪團伙也落入法網。
據了解,公安機關在此案中扣押的假藥多達幾百種,“功效”龐雜且大都冒充的是常用藥品,包裝、使用說明書都與真藥無二,大多在正規藥店、診所出售。
著名醫改專家魏子檸在接受《中國產經新聞》記者采訪時認為,當前,大量假藥不僅流入了網上、農村,甚至還流入了正規的藥店。監管層在這方面的監管其實難度是比較大的,同時,其監管也相對薄弱些。
監管力度逐步加大
山東日照市某鄉鎮的王女士前不久剛剛做完心臟手術。王女士的女兒劉然(化名)告訴《中國產經新聞》記者,她的母親是做第二次心臟支架,第一次做的時候是在幾年前做的,因種種因素,那時候她的母親沒有醫保,所以心臟支架全部是自費花了十多萬元,而這一次做支架因為這邊的農村也納入到了醫保,所以這次做心臟手術只花了7萬元。
“一般老人家類似這種大病才能到市里看病,但是平時家人有個頭疼腦熱的(指的是感冒、頭疼等一些小病種)就不可能到市里的大醫院打針或者開藥,都是在村里的診所拿點藥。但目前有個問題是,村里診所的藥感覺不太對勁。”劉然說,有一次,她父親得了急性胃炎,就到診所拿了點藥吃,但吃后止痛的效果并不明顯,后來又給她打電話,她從市里的藥房開了同樣廠家及一樣品牌的藥,父親吃完她在市里買的藥后,疼痛也止住了,所以她懷疑村里的小診所賣的有可能是假藥。
前不久,據央視新聞頻道報道稱,江西警方破獲了一起售賣假藥的案件,現場一卡車一卡車的假藥運輸回來,其中,包括孕婦所服用的葉酸,老人用的風濕膠囊等,光現場查獲的假藥和原料就有整整6噸多,賺取受害者資金超過1400多萬元。
該新聞還報道稱,今年1月30日,江西吉水縣公安局治安大隊聯合縣市場監督管理局在吉水縣文峰鎮某診所內查獲了金易通丸、風濕骨友靈、特效筋骨康等藥品,經過檢測均屬假藥。
藥品出現問題的不僅僅上述兩列,最近的一次問題藥品曝光來源于國家藥監局的一則通報。據國家藥品監督管理局通報顯示,根據線索,該局組織對長春長生生物科技有限責任公司開展飛行檢查,發現該企業“凍干人用狂犬病疫苗”生產存在記錄造假等嚴重違法違規行為。
記者在梳理資料時也了解到,雖然長春長生生物科技有限責任公司生產的“凍干人用狂犬病疫苗”存在問題,但幸運的是,本次飛行檢查所有涉事批次產品尚未出廠和上市銷售,全部產品已得到有效控制。
魏子檸說,近些年來,監管層對于假藥、劣質藥的打擊力度越來越大,而藥品管理法對生產、銷售假藥和劣質藥的監管是有明確規定的,并且處罰力度也在逐步提高。
據了解,針對此次長春長生生物科技有限責任公司的違法違規行為,國家藥監局和吉林省食藥監局分別對公司全資子公司作出了多項行政處罰共計91億元。
去疴的“猛藥良方”
事實上,監管層在查處假藥、劣質藥或有問題的假藥背后,也暴露出我國在藥品安全監管領域還存在不少漏洞。近些年來,一些制藥企業及個人為了獲取暴利,導致藥品安全質量問題及造假的案例頻發。不過,值得欣喜的是,對于吉林長春長生公司的問題疫苗案件發生后,也引起了中央政府的高度重視,由此也進一步影響了藥品管理修正法的修訂進程。稍早之前,記者在全國人大常委會公布的2018年度的全國人大常委會立法工作計劃中注意到,藥品管理法修正案并不在其中。
國家藥監局局長焦紅指出,吉林長春長生公司問題疫苗案件發生后,習近平總書記作出重要指示,要求立即調查事實真相,一查到底,嚴肅問責,依法從嚴處理,強調要始終把人民群眾的身體健康放在首位,以猛藥去疴、刮骨療毒的決心,完善我國疫苗管理體制。 10月22日召開的第十三屆全國人大常委會第六次會議上,國務院就提請審議《中華人民共和國藥品管理法(修正草案)》(以下簡稱:修正草案),擬針對問題疫苗案件暴露出的突出問題,對實施藥品上市許可持有人制度和推進審批制度改革以及藥品監管制度等方面進行了修改。
據了解,修正草案擬從四方面加大對違法行為的處罰力度,解決違法成本低、處罰力度弱的問題。一是全面加大對違法行為的行政處罰力度。二是落實“處罰到人”要求,對嚴重違法行為的責任人進行處罰。三是結合本次修法相應補充了藥品上市許可持有人的法律責任以及違法報告、召回等新設義務的法律責任。四是細化并加重對地方政府負責人和監管人員的處分,對隱瞞、謊報、緩報藥品安全事故等行為規定了嚴格的處分。在疫苗方面,修正草案不僅強化了對疫苗的監管,還提出了新的規定。例如,擬明確規定疫苗、血液制品、麻醉藥品、精神藥品、醫療用毒性藥品不得委托生產。不過,國務院藥品監督管理部門規定可以委托生產的情形除外。
“修正草案中明確要求藥品供應與保障,對藥品的研發、生產、流通、使用、評價、監管等,體現了國家對藥品進行全過程監管的治理思路。”魏子檸表示,把建立健全以市場需求為導向的藥品審評審批制度,鼓勵研究和創制新藥等寫入了這部法律,更加體現了國家在研發創新藥品的力度。這部法律如正式發布后,將給各類藥企和機構戴上“緊箍咒”。例如,企業的研發創新,轉型升級以及藥品質量都會得到改善,從法律層面上講,這部法律可以保障藥品質量,讓群眾吃上“定心丸”。
]]>